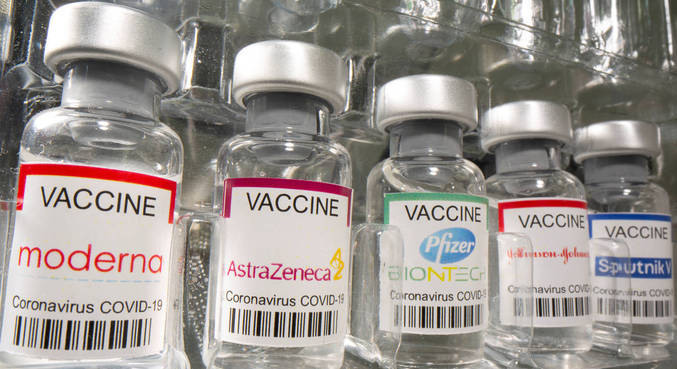
Na semana passada, a União Europeia anunciou que só aceitará a entrada de turistas que tomaram alguma das vacinas contra covid-19 já aprovadas pelo bloco: os imunizantes da Pfizer, Oxford/Astrazeneca, Johnson e Moderna.
Dentre elas, a vacina de Oxford é distribuída em larga escala no Brasil e o país recebeu um lote de 1 milhão de doses da Pfizer no final de abril. Ainda não há previsão de quando chegarão as doses da Moderna. No caso da Johnson, existe a previsão de entrega a partir de julho.
A outra vacina aprovada no Brasil, a CoronaVac, ainda está sendo analisada pela Agência Europeia de Medicamentos, que anunciou na última terça-feira (4) que começaria os estudos do imunizante da Sinovac para aprovação ou recusa.
Com isso, aqueles que foram imunizados com a CoronaVac ficam em dúvida se poderão viajar para algum dos países que compõem o bloco num futuro próximo, quando as restrições contra viajantes brasileiros foram suspensas. Por enquanto, turistas vindos do Brasil não podem entrar no Espaço de Schengen, um grupo de 26 países com fronteiras abertas entre si, por causa da variante brasileira.
Segundo o professor de Saúde Pública da USP (Universidade de São Paulo) Fernando Aith, os países que formam a União Europeia têm o direito de decidir quem pode entrar em seus territórios e quais as vacinas que eles aceitam.
“Isso faz parte do exercício de soberania desses países”, explica. “Os governos têm plenos poderes para decidir quem entra e quem não entra”.
Na segunda-feira (3), a Comissão Europeia propôs que o bloco aceitasse pessoas plenamente imunizadas com outros fármacos. Ainda não foi definido quais serão os próximos passos das autoridades.
A aprovação das vacinas
A Agência Europeia de Medicamentos é um dos órgãos reguladores mais importantes no mundo, e um dos mais rígidos.
Para uma vacina ser aprovada, são analisados os dados da fase 3 dos ensaios clínicos e todos os dados fornecidos pelos fabricantes. Neles, é necessário estar claro quantas pessoas tomaram o imunizante, os efeitos colaterais e os estudos, esclarece o professor.
Nas análises, são medidas a eficácia, qualidade e segurança da vacina. Para os europeus, as vacinas precisam ter mais de 50% de eficiência, o mesmo índice aprovado pela OMS. A CoronaVac chega a 62,3% de eficácia, segundo testes.
Essas empresas também podem publicar os estudos e resultados em revistas científicas indexadas, o que corrobora com a eficácia da vacina e reputação do fármaco.
“Na publicação em revistas científicas, outros cientistas leram os resultados e viram que eles comprovam a eficácia”, diz Aith. “Essas revistas têm exigido cada vez mais a abertura dos bancos de dados.”
Apesar de não ser um processo relevante durante a análise das agências reguladoras, a publicação nas revistas científicas aumenta o acesso desses dados e resultados para toda a comunidade e aqueles que se interessarem pela especificação de cada vacina.
A Anvisa, órgão regulador brasileiro, segue o modelo europeu de análises e aprovação. Até agora, o Brasil só não aprovou uma vacina que está sendo usada pelo mundo, a Sputnik V, produzida na Rússia.
Para quem tomou a CoronaVac e pretende viajar ao Velho Continente, será necessário aguardar para ver os próximos passos do bloco.
Mesmo com a decisão conjunta da União Europeia, cada país tem a autonomia para decidir se vai aceitar cidadãos imunizados com outras vacinas, ou não. Então, é possível que um país libere a entrada de brasileiros e outros barrem os turistas.
“Tem que acompanhar cada país e as vacinas que eles vão aprovar”, recomenda o especialista.
O Brasil pode tentar negociar com as autoridades europeias para abrir uma brecha, ou então, aplicar o princípio da reciprocidade e não permitir que europeus entrem no país.
Com a entrada do pedido da Sinovac, é possível que o bloco aceite a vacina e autorize a vacina, o que permitirá que todos os cidadãos vacinados possam entrar tranquilamente na Europa, desde que apresentem comprovantes da vacina.
Fonte: R7
Créditos: R7