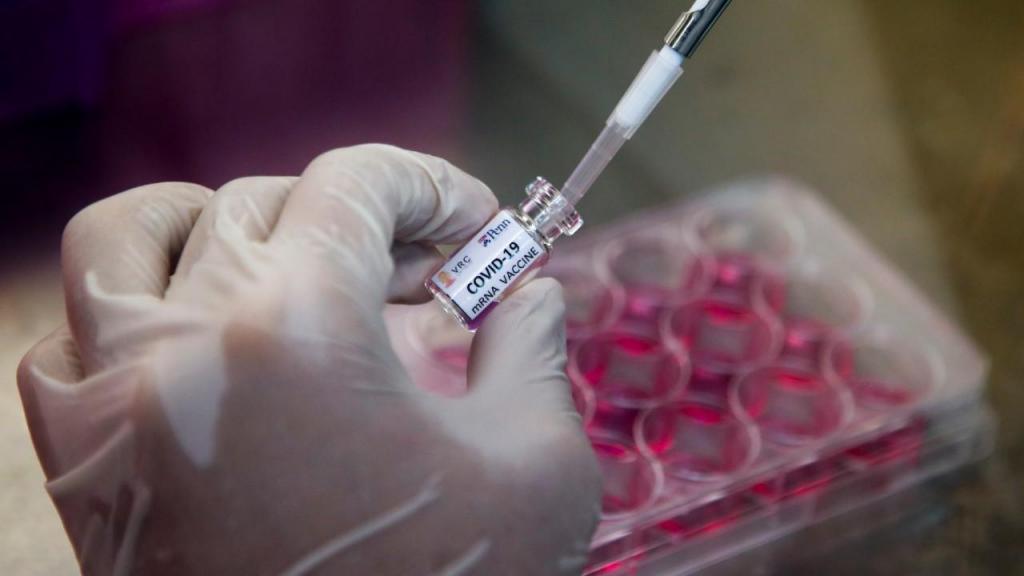
Os testes das vacinas contra o coronavírus desenvolvidas pela AstraZeneca e pela Johnson & Johnson, ambas já na última fase de testagens, foram retomados nos Estados Unidos. Na sexta-feira, 23, as empresas disseram que as doenças graves detectadas em alguns voluntários pareciam não ter relações com os imunizantes.
Reguladores federais de saúde deram à AstraZeneca o sinal verde após uma pausa de seis semanas, concluindo que não havia evidência de que a vacina experimental tenha diretamente causado os efeitos colaterais neurológicos relatados em dois voluntários. A notícia foi confirmada pelo The Wall Street Journal.
A Johnson & Johnson afirmou que seus testes, que foram interrompidos por 11 dias, seriam retomados após terem descoberto que um “grave evento médico” em um voluntário não teve “nenhuma causa clara”. Em uma entrevista, o diretor científico da empresa, Paul Stoffels, disse que ninguém na companhia sabia se o voluntário tinha recebido o placebo ou a vacina, como uma forma de preservar a integridade dos testes.
Um porta-voz da Food and Drug Administration (FDA, órgão de regulamentação dos EUA) se recusou a comentar a retomada dos testes.
Luciana Borio, ex-diretora científica da FDA, acolheu com prazer os anúncios, citando a necessidade urgente de que várias vacinas continuem na corrida por um produto que possa proteger a população global do coronavírus, que já matou mais de 1 milhão de pessoas no mundo.
“A demanda por vacinas seguras e eficazes contra a covid-19 excede qualquer capacidade de produção de um único fabricante”, disse Borio. “Realmente precisamos de muitos no campo.”
A AstraZeneca e a Johnson & Johnson são duas das quatro empresas agora no estágio final de ensaios clínicos nos Estados Unidos para vacinas experimentais contra o coronavírus. Ambas as empresas estão usando um adenovírus, que normalmente causa resfriados inofensivos e é construído de modo a conduzir um gene do coronavírus para dentro de células humanas.
Seus dois maiores competidores, a Moderna e a Pfizer — também em estágios avançados de testagens — estão usando como alternativa uma tecnologia baseada em um material genético conhecido como mRNA (RNA mensageiro). Transmitido para as células humanas, o mRNA impulsiona a produção das proteínas do coronavírus, provocando uma resposta imune.
A AstraZeneca moveu-se rapidamente para os ensaios clínicos, registrando milhares de voluntários ao redor do mundo em países como Brasil, Índia, África do Sul e Grã-Bretanha. Uma testagem ampla e já na fase final começou nos Estados Unidos no fim de agosto. Mas todos os estudos foram interrompidos dias depois, em 6 de setembro. Um voluntário que recebeu a vacina no Reino Unido supostamente teve sintomas de mielite transversa, ou inflamação da medula espinhal, causando uma pausa global nos esforços da empresa.
O incidente levantou preocupações entre especialistas, que notaram que um evento neurológico adverso parecido, relatado meses antes, havia ocorrido em outro voluntário vacinado. Apesar de esse evento anterior ter impulsionado sua própria pausa aos ensaios da AstraZeneca, um conselho de segurança independente acabou por determinar que ele não tinha relações com a vacina, permitindo a retomada das testagens.
Após a segunda interrupção da AstraZeneca em setembro, estudos no exterior foram rapidamente retomados na maioria dos países. Mas o hiato persistiu nos EUA, com poucos detalhes publicados sobre o motivo para isso.
De acordo com dois especialistas em vacina familiarizados com a situação e que não foram autorizados a discuti-la publicamente, a FDA não vinculou diretamente a vacina às duas doenças neurológicas, apesar de não poderem descartar a hipótese. A agência aconselhou a empresa a alertar os voluntários do estudo sobre sintomas relacionados, como fraqueza e dormência que poderiam apontar para um caso moderado de mielite transversal, afirmaram os especialistas.
A Johnson & Johnson começou a fase 3 do seu estudo clínico em 60 mil voluntários em setembro. Em 12 de outubro, a empresa anunciou sua própria interrupção nas testagens, citando preocupações de que uma doença havia ocorrido também em um de seus voluntários. A empresa tem se mantido majoritariamente quieta sobre os detalhes do incidente.
“Há muitos fatores possíveis que poderiam ter causado o evento”, disse a empresa. “Baseado na informação coletada até agora e na opinião de especialistas independentes, a empresa não encontrou evidências de que a candidata a vacina causou o evento.”
Eventos adversos não são incomuns em ensaios de vacina de larga escala. Em alguns casos, eles são causados por uma vacina. Mas investigações geralmente revelam que eles são coincidência — uma simples questão de chance.
Agora que os estudos estão sendo retomados, disse Borio, mudanças podem precisar ser feitas “para aumentar as medidas de segurança”, pelo menos no caso da AstraZeneca, que, por sinal, provavelmente vai precisar de monitorar seus voluntários para sintomas neurológicos moderados agora que há um precedente.
Com base em eventos recentes, “parece que não havia nenhuma preocupação com a segurança” nos dois episódios neurológicos, disse Maricar Malinis, especialista em infectologia na Universidade de Yale. O recomeço do estudo, ela enfatizou, deveria ser considerado uma notícia positiva e uma indicação que os reguladores suas devidas diligências.
Antes das pausas,ambas as empresas tinham indicado que iriam provavelmente submeter suas vacinas à autorização de emergência da FDA em apenas alguns meses — talvez até o final do ano. Ainda permanece incerto o quanto esses planos agora foram alterados à luz dos atrasos nos ensaios. Os resultados dos estudos de fase final da AstraZeneca ainda são esperados para o final deste ano, de acordo com um comunicado.
Stoffels, da Johnson & Johnson, afirmou que uma pausa não iria adiar muito a previsão da empresa. “Nós temos a habilidade de correr atrás do tempo perdido”, disse. “Mas se houver uma demora, é no prazo de uma ou duas semanas.”
Fonte: Estadão
Créditos: Estadão